酸が解離して生じたプロトン(H+)は通常孤立しては存在せず、たとえば水中では水分子に結合してオキソニウムイオンH3O+となり、さらにこのH3O+は周囲の水分子に水素結合を介して取り囲まれます。ここでプロトンは正電荷を持っているため、その電荷が作る電場は周囲の水分子を通常よりも強く分極させます(Oδ--Hδ+間の電荷の偏りδ+/δ-が大きくなります)。水分子間の水素結合の強度はこのO-H間の分極の大きさに影響を受けるため(より強く分極するとより強い水素結合を作ります)、結局H3O+を取り囲む水分子はこれらをさらに外側から取り囲む水分子と通常よりも強い水素結合を作ることになります。このようにプロトンの電荷にはその周囲にある水素結合の強度を増強する効果があります。
それでは、この増強効果は実際周囲の何分子(中心にプロトンが付加した分子をおいて、そこから何層目の分子)にまで及ぶのでしょうか?これを実験的に決めるためには、液体中のプロトン周辺のごく微小な領域のみを選択して観測せねばならず、非常に困難です。そこで私たちは、1個のプロトン(余剰プロトン)と予め限られた数の分子からなる小集団(「分子クラスター」と呼ばれます)を真空中に取り出し、このクラスターに含まれる分子の個数を変えることにより、プロトンの周りに存在する分子の数を厳密に制御して、プロトンの影響が周囲の水素結合に及ぶ範囲を決定することを試みました。具体的には、メタノール(CH3OH、以下MeOH)が最も単純な、1次元的な水素結合のつながり方を好むので、これを対象とし、余剰プロトンを含むプロトン付加メタノールクラスターH+(MeOH)nを真空中に発生させました。H+(MeOH)nは図に示すように、中心に余剰プロトンが付加したCH3OH2+(メタノールのオキソニウムイオンであり、ヒドロニウムイオンやアンモニウムイオンに類似します)が存在し(黄色で強調された部分)、そこからn-1個のメタノール分子が水素結合により結ばれて1次元的に連なります。この水素結合による連なりの末端に位置するメタノールにベンゼン分子(C6H6)を付着させます。ベンゼンには実は弱い水素結合性があり、メタノールの水酸基(紫色で強調された部分)の先端に芳香環面を向けて付着します。すると、この水酸基のO-H結合の振動が水素結合の強さを反映して変化し、その変化を目に見えない領域の光である赤外光の吸収波長の変化として観測することが出来ます。様々なメタノールの分子数からなるクラスターで測定を行ったところ、およそ7分子以上のメタノールが連なると、末端のメタノールが作る水素結合の強度が余剰プロトンが無い場合とほぼ同じになることが分かりました。これは中心のオキソニウムイオン(余剰プロトン)による水素結合の増強効果が及ぶ範囲が左右に3分子程度までに留まることを意味しています。今回の結果から、オキソニウムイオンの周囲に3次元的な水素結合のかご(水和殻)を形成する水の場合も、中心イオンからの水素結合増強効果は3層目の水和殻でほぼ止まることが予想されますが、確証を得るためには更なる研究が必要です。
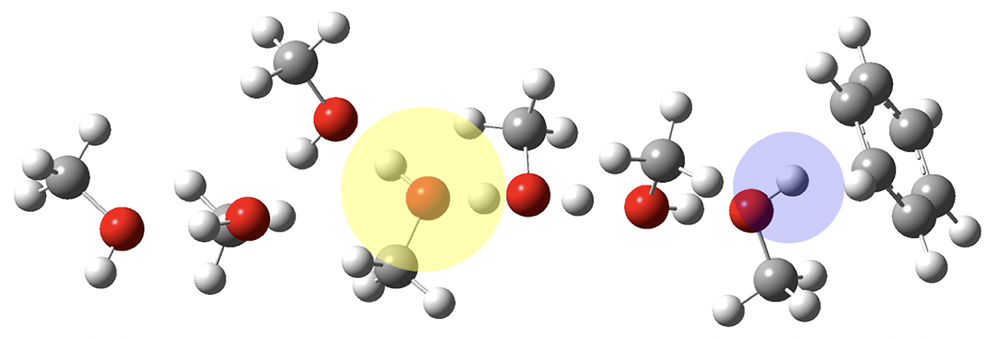
ベンゼンが末端に付着したプロトン付加メタノールクラスター
黄色部分がオキソニウムイオン、紫部分がベンゼンに水素結合した水酸基を示している。
(論文情報)
(掲載日:2022年5月17日)
